免疫组库(Immune Repertoire,IR)是指机体内 T 淋巴细胞和 B 淋巴细胞多样性的总和,反映机体免疫系统在特定时间段内应对外界刺激应答的能力。基于 10X Genomics 的单细胞系统,可实现高通量的单细胞转录组和 V(D)J 测序。不但可以将 TCR/BCR 双链匹配,而且能够同时获得基因表达信息。
技术原理
10X Genomic 单细胞免疫组库测序与单细胞 RNA 测序一样,通过微流控系统将带有条形码和引物的凝胶珠与单个细胞包裹在油滴中;接下来在每个油滴内,凝胶珠溶解,细胞裂解释放 mRNA,通过逆转录产生带有 10X barcode 和 UMI 信息的 cDNA。破油(Breaking Emulsions)之后,cDNA 一分为二,后续同时进行基因表达和免疫组库的文库构建。其中 TCR 或者 BCR 的 V(D)J 序列通过设计在 C 区的巢式引物进行 PCR 富集;而 mRNA 的信息,与 10X Genomics 3’mRNA 文库不同,保留的是 5’端的信息。测序后即可一次性获得大量单细胞的基因表达和免疫组库数据。
图 5’mRNA 与 TCR/BCR 同时建库
技术优势
●通量高
一张芯片具有 8 个独立的通道,可供 8 个样本同时上机,每个通道最高可捕获 10000 个细胞。
● 分辨率高
可获得真正单细胞水平的的免疫组库信息,并且可匹配 TCR/BCR 的双链。
●信息全面
可同时获得单个细胞匹配的 mRNA 和 TCR/BCR 信息。
文库结构
● 5’gene expression 文库:
图 10X Genomics 5’gene expression 文库示意图
●V(D)J 文库:
图 10X Genomics V(D)J 文库示意图
建议测序深度及参数
指标 | 参数 |
测序深度 -5’mRNA | 50,000~100,000 reads/cell |
测序深度 -TCR/BCR | 5,000~10,000 reads/cell |
测序类型 | PE150 |
样本要求
● 类型:
新鲜组织,原代细胞,细胞系等。
● 来源:
血液提取、磁珠富集、流式富集、组织解离等。
● 样本量及其它质控要求:
| 样本类型 | 要求 |
| 细胞悬液 | > 10* 目标细胞个数(最少 10,000 个细胞); |
| 活率 >80%; | |
| 浓度 500-1,000 个细胞 /ul; | |
| 细胞间无粘连(成团率 <5%); | |
| 无大于 40um 的细胞碎片或其他颗粒物; | |
| 不存在逆转录抑制剂和非细胞的核酸分子。 | |
| 血液 | EDTA 抗凝的全血(不可肝素抗凝),>5ml。 |
| 组织 | 0.3cm × 0.3cm(不超过 0.5 × 0.5cm)的新鲜组织,4~5 块。 |
| 样本类型 | 要求 |
| 细胞悬液 | 最好现场制备,如要运输,建议使用伯豪生物自主研发的单细胞保护液,4°C 运输,48 小时内送达伯豪生物实验室。 |
| 血液 | EDTA 抗凝的全血,4°C 运输,2 小时内送达伯豪生物实验室;或提取 PBMC 后冻存,干冰运输。 |
| 组织 | 建议使用伯豪生物自主研发的单细胞组织保护液,4°C 运输,48 小时内送达伯豪生物实验室。 |
应用方向
★肿瘤微环境
★ 自身免疫性疾病
★ 感染性疾病
★ 器官、骨髓移植
★ 抗体开发
应用案例
1、肝癌免疫微环境
2017 年,北京大学张泽民教授课题组通过大规模单细胞测序技术对肝癌相关 T 淋巴细胞进行了分析,首次在单细胞水平上描绘肝癌微环境中免疫图谱。研究者收集了 6 例肝癌患者的外周血,癌旁正常组织、肝癌组织作为实验样本,然后从各类样本中用流式分选出 CD3+CD8+(cytotoxic T cells,Tc)细胞,以及 CD4+CD25-(Helper T cells,Th)细胞和 CD4+CD25+(regulatory T cells,Tregs)细胞,并进行了单细胞转录组测序和单细胞 TCR 测序,总共获得 5063 个单细胞的数据。其中,单细胞水平分析 TCR 序列发现,在肿瘤侵润的 exhausted T 细胞和 Tregs 细胞中,观察到 TCRs 发生了重复使用。在肿瘤组织中含有相同 TCR 的 T 细胞比例较高,而在外周血和正常组织中比例较低,这说明在肿瘤中的 exhausted T 细胞和 Tregs 细胞发生了克隆扩增。并且相比于早期病人,晚期病人中 T 细胞的克隆扩增更加明显。
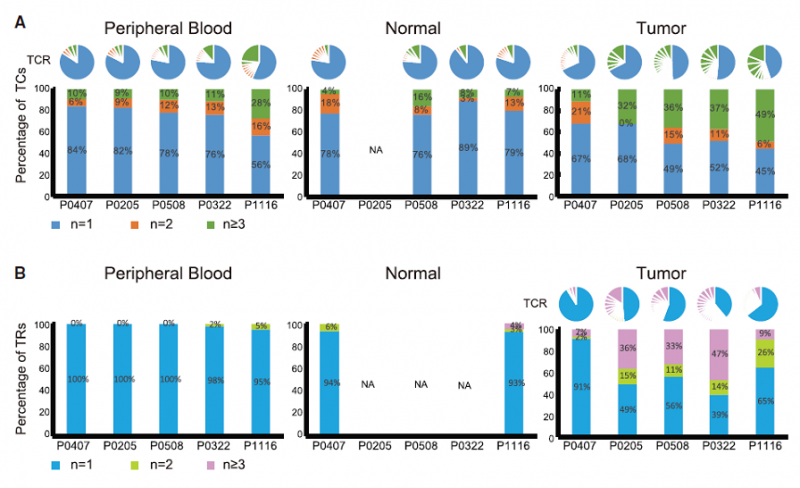
图 肝癌中 T 细胞的克隆扩增
2、黑色素瘤免疫微环境
2019 年发表在 Cell 上发表的一篇论文,对 25 个黑色素瘤患者肿瘤中总共 46,621 个免疫细胞进行了单细胞 RNA 和 TCR 测序。这些细胞被分成 7 个大群,包括 T 细胞(CD3),NK 细胞(KLRD1),树突细胞(DCs;CD1C),巨噬细胞(C1Q),单核细胞(VCAN),B 细胞(CD19),和浆细胞(immunoglobulins)。初始 T 细胞高表达 IL7R, CCR7 和转录因子 TCF7,特异性表达的基因整体来说比其它类型的细胞少。而非初始 T 细胞具有很高的异质性,其中一小群是记忆 T 细胞,大部分细胞是过渡性 CD8 T 细胞(transitional CD8 effector T),细胞毒性 CD8 T 细胞(cytotoxic CD8 effector T)和丧失功能的 CD8 T 细胞(dysfunctional CD8 T cells),高表达 PD- 1 和 LAG3。这些细胞类群的边界是模糊的,提示转录的梯度表达是造成 T 细胞异质性的原因。CD4 T 细胞主要有高表达 FOXP3 的 Treg,滤泡辅助 T 细胞(CXCL13 表达),以及一小群高表达免疫检查点分子的细胞(dysfunctional CD4 T cells)。分析每名患者的免疫细胞组成,发现大部分 T 细胞类群在患者中都存在,但是病人之间不同细胞类群的丰度有很大差异。丧失功能的 CD8 T 细胞的负荷可能是黑色素瘤最本质的特征。
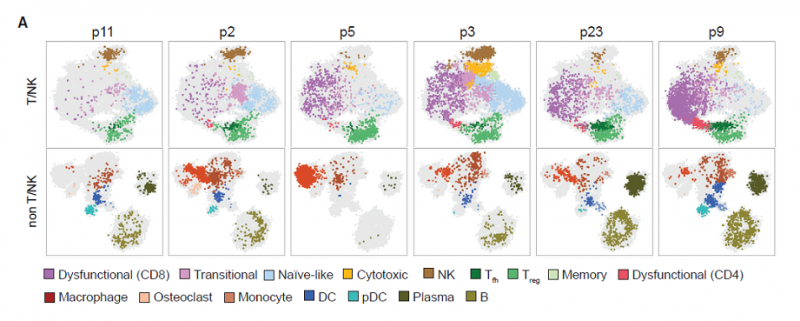
图 病人间免疫微环境异质性
通过分析 T 细胞的 TCR 序列,发现不同病人的 TCR 克隆型构成差异较大。一些大的克隆中细胞类型也不同,主要表现为丧失功能的 CD8 T 细胞的富集和初始 T 细胞的缺失。患者中丧失功能的 CD8 T 细胞的比例与 T 细胞的扩增程度呈现正相关。通过计算每个细胞的增殖分数,发现丧失功能的 CD8 T 细胞有最高增殖细胞比例,比初始 T 细胞高出 10 倍。
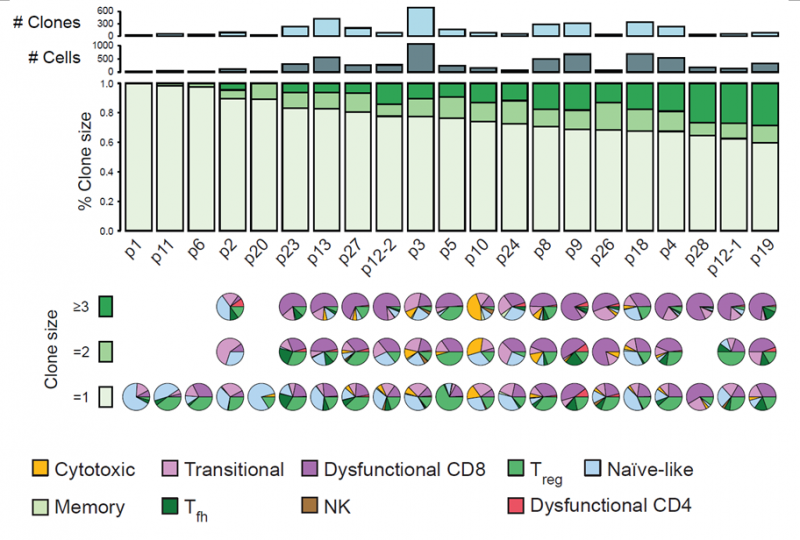
图 黑色素瘤中 T 细胞的克隆扩增
3、免疫治疗
靶向 PD-1/PD-L1 通路的免疫检查点抑制剂的出现,给癌症的临床治疗带来了革命性的变化。然而 PD- 1 抗体的抑癌机制,并不完全为人所知。其中一个非常关键的问题是,PD- 1 抗体的抑癌效果,究竟是依赖于在治疗前就存在于肿瘤中的浸润淋巴细胞的再激活,还是治疗之后,肿瘤外的杀伤 T 细胞进入肿瘤?这个问题,目前也是不清楚的。来自斯坦福大学医学院的研究团队,从接受 PD- 1 抗体治疗前后的基底细胞癌(BCC)或鳞状细胞癌(SCC)患者身上采集了 79046 个细胞(包括癌细胞和各种免疫细胞),进行了单细胞 RNA 测序和 TCR 测序。基于单细胞 RNA 测序结果,细胞分成 19 个亚群。
本研究的重点是免疫细胞,尤其是浸润性免疫细胞,以及治疗前后的变化,以了解克隆性 T 细胞对 PD- 1 抗体治疗的反应。因此研究人员把所有的 33106 个肿瘤浸润性 T 细胞做了个更细致的分类,包括表达 CD4 的调节性 T 细胞(Treg)细胞,滤泡辅助性 T(TFH)细胞,T 辅助细胞 17(TH17)细胞;以及表达 CD8 的幼稚细胞,记忆 T 细胞,效应记忆 T 细胞,活化 T 细胞,慢性活化 / 耗竭 T 细胞,中度耗竭 / 活化细胞。进一步分析发现,在 PD- 1 抗体治疗之后,滤泡辅助性 T 细胞,以及活化,耗竭和耗竭 / 活化的 CD8 阳性 T 细胞的频率增加,并且耗竭 T 细胞的克隆水平明显更高。更为让研究人员感到意外的是,对于同一个患者而言,治疗后记忆 T 细胞和效应 T 细胞频繁转换为活化状态,但是治疗前的耗竭 T 细胞却没有变成治疗后的非耗竭表型。这表明,即使在 PD- 1 抗体治疗后,已经耗竭的肿瘤浸润 T 细胞也很难变成活化状态了。
图 治疗前后 T 细胞的状态转换。
此外,研究人员还观察到一个有趣的现象,PD- 1 抗体治疗后才出现的耗竭性 T 细胞表现出了新的 TCR 特异性。为了分析外周血中是否存在新发现的肿瘤浸润性 T 细胞,研究人员给患者的血液样品做了 TCR 测序,发现 35.5% 新肿瘤浸润性 T 细胞可以在 PD- 1 抗体治疗后的外周血中找到,而在治疗前的外周血中只能找到 11.8% 的新肿瘤浸润性 T 细胞,不过治疗前的肿瘤里面却没有新肿瘤浸润性 T 细胞。
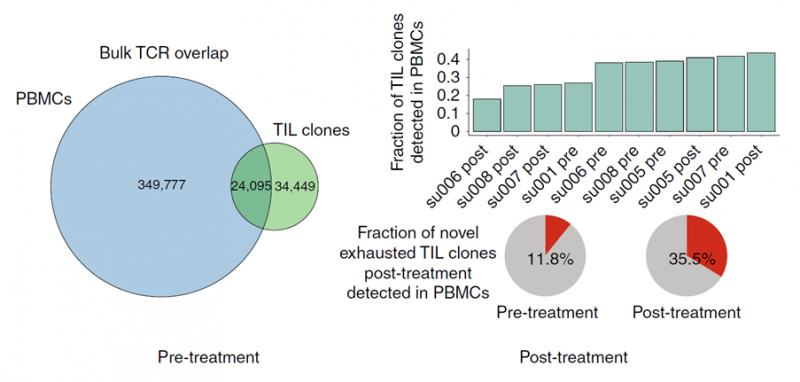
图 新发现的肿瘤浸润性 T 细胞在外周血中的比例
总的来说,与“冷”肿瘤相比,“热”肿瘤之所以响应 PD- 1 抗体的治疗,可能是由于“热”肿瘤自身的特性,让它能够不断吸引新 T 细胞进入,而不是重新激活已有的肿瘤浸润性 T 细胞。这项研究让我们对免疫检查点抑制剂的作用机制有了新的认知,这对临床治疗和疗效的检测都有一定的价值和意义。
上海伯豪生物技术有限公司(以下简称“伯豪生物”)2008年12月成立,是一家以科技服务、疾病与健康检测、分子检测产品的开发和生产为主营业务的高新技术企业。公司形成了面向科研和临床的系统技术服务平台,提供全基因组测序、生物信息分析、标志物筛选和分子检测验证、基因功能验证科研一站式服务,同时提供试剂盒开发、生产以及检测应用的转化医学的临床一站式服务。伯豪生物携手各参控股子公司重庆伯豪医学检验所(临床医学检测专业子公司)、伯豪医药(医疗器械经营专业子公司)和迅伯生物(产品研发和GMP生产专业子公司)共同开启“专业服务成就科学发现,产业布局构筑精准医学”的新篇章。 公司于2011年12月6日获得高新技术企业认定。2012年3月获批浦东新区企业研发机构。公司拥有自主知识产权的发明专利、实用新型专利和应用于芯片、新一代测序等数据分析的软件著作权专利(其中发明专利6项,实用新型专利2项,软件著作权25项,正在申请专利7项)。目前,公司拥有六大服务平台:生物样品分析平台、微阵列芯片平台、新一代测序平台、生物标志物平台、分子检测平台、生物信息平台,凭借高标准的技术平台和多样化的服务等竞争优势,公司向国内外企业和相关单位提供系统的生物学研究全面解决方案。上海伯豪为多达18家跨国制药企业(包括排名前10位的跨国制药企业)和超过3000家的国内科研机构、医院等提供基因表达谱、基因分型、比较基因组学、DNA甲基化、miRNA、生物标志物筛选及确认、生物信息等技术服务。公司拥有一支以上海为基础,辐射全国的强大市场营销队伍和销售网络,已设立华北、华南、华东三个大区十四个办事处,推广公司的主导技术服务、代理产品,快速提升公司品牌的知名度,扩大影响力。过去10年承接项目数超过15000个,用户单位3000家以上,协助客户发表SCI论文1400余篇(平均IF5),全面推动了中国基因组学服务产业的发展。公司的系统化技术平台和高质量的服务体系得到了广大客户青睐和合作伙伴的度评价和认可。公司通过了ISO 9001:2008质量体系认证,采用SOP(Standard Operation Procedure)规范操作文件来控制样本品质、检测品质和数据结果品质,目前已建立了SOP管理文件128个。公司于2012年获得诺华优秀服务供应商奖,公司是Affymetrix公司在中国第一家认证的服务提供商,是Illumina NGS认证服务供应商,还是Agilent公司和ABI公司在国内唯一认证的服务提供商,并先后被授予“Agilent公司亚太区最佳服务供应商”、“Affymetrix公司优秀服务商”称号。上海伯豪将持之以恒地利用高端的现代化仪器设备、多项成熟完善的技术平台、高素质的技术团队、国际水平的商业化服务流程、积极进取的经营理念,为广大客户提供持续、高效和稳定的技术支持和服务。